Nytt om forskning
SveDem följer upp nya demensläkemedel
Kvalitetsregistret SveDem har tagit fram en modul för nya demensläkemedel. Den kan börja användas redan i slutet av året, om europeiska läkemedelsmyndigheten godkänner den svenskutvecklade antikroppen lecanemab.
Den nya modulen, som har tagits fram i samarbete med kompetenscentrat Uppsala Clinical Research Center, kan ge ökade kunskaper om läkemedlens effekter.
 – Den ger oss möjlighet att undersöka en stor population som använder de nya läkemedlen och som vi kan följa över en längre tid. På så sätt kan vi få mer kunskap om effekter som inte fångas upp av läkemedelsbolagens betydligt mindre studier och som man därför inte känner till, säger Maria Eriksdotter, registerhållare för SveDem, professor i geriatrik, Karolinska Institutet, och överläkare på Karolinska Universitetssjukhuset, Huddinge.
– Den ger oss möjlighet att undersöka en stor population som använder de nya läkemedlen och som vi kan följa över en längre tid. På så sätt kan vi få mer kunskap om effekter som inte fångas upp av läkemedelsbolagens betydligt mindre studier och som man därför inte känner till, säger Maria Eriksdotter, registerhållare för SveDem, professor i geriatrik, Karolinska Institutet, och överläkare på Karolinska Universitetssjukhuset, Huddinge.
Samlar in patientdata
Kvalitetsregistret SveDem – världens största demensregister – samlar en mängd olika data om patienter, från att diagnosen ställs till att personen flyttar till ett särskilt boende. I stort sett alla minnesmottagningar i landet är anslutna men även många vårdcentraler och särskilda boenden registrerar patientdata i SveDem.
De alzheimerläkemedel – kolinesterashämmare och memantin – som idag förskrivs ingick i SveDem redan från registrets startår 2007. De data som analyserats uppvisar små men positiva och långvariga effekter på kognitionen av kolinesterashämmare. Maria Eriksdotter pekar på bland annat en påtagligt lägre mortalitet (dödlighet) jämfört med de som inte har fått kolinesterashämmare förskrivna.
Vad skiljer då den nya läkemedelsmodulen mot det befintliga sättet att registrera läkemedel i SveDem?
Mer detaljerad
– Den nya modulen är betydligt mer detaljerad. Här registreras inte bara när läkemedlet börjar förskrivas, vilken dos och datum för utsättning. Det innehåller även frågor om varför dosen korrigeras, varför läkemedlet sätts ut och så vidare samt uppföljning av kognition och funktion. Till detta kommer de särskilda krav som är förenade med olika läkemedel i framtiden, säger Maria Eriksdotter.
Den svenskutvecklade antikroppen lecanemab kan bli det första nya alzheimerläkemedlet i Sverige på drygt 20 år, om det får klartecken av europeiska läkemedelsmyndigheten (EMA). Efter ett eventuellt godkännande kommer sannolikt att följa en rad villkor för förskrivningen.
– Det kan handla om krav på magnetröntgenundersökning och tätare uppföljningar med instrument som bedömer kognition och funktionsförmåga. Exakt vad det kommer att handla om vet vi ju inte ännu men det är den typen av data som kan registreras och följas upp i den nya modulen, säger Maria Eriksdotter.
Minnesmottagningarna först ut
Lecanemab är inte ett läkemedel som man tar genom munnen. Det ges som dropp varannan vecka och kräver alltså ett besök på en sjukvårdsmottagning.
– Troligen kommer minnesmottagningarna ta hand om detta, om det skulle bli aktuellt. Då är det också minnesmottagningarna som ska registrera i den nya läkemedelsmodulen. Men inget hindrar att vi öppnar modulen även för primärvården, om det skulle behövas, säger Maria Eriksdotter.
Text: Magnus Westlander
Foto (porträtt): David Thunander
Den nya modulen, som har tagits fram i samarbete med kompetenscentrat Uppsala Clinical Research Center, kan ge ökade kunskaper om läkemedlens effekter.
 – Den ger oss möjlighet att undersöka en stor population som använder de nya läkemedlen och som vi kan följa över en längre tid. På så sätt kan vi få mer kunskap om effekter som inte fångas upp av läkemedelsbolagens betydligt mindre studier och som man därför inte känner till, säger Maria Eriksdotter, registerhållare för SveDem, professor i geriatrik, Karolinska Institutet, och överläkare på Karolinska Universitetssjukhuset, Huddinge.
– Den ger oss möjlighet att undersöka en stor population som använder de nya läkemedlen och som vi kan följa över en längre tid. På så sätt kan vi få mer kunskap om effekter som inte fångas upp av läkemedelsbolagens betydligt mindre studier och som man därför inte känner till, säger Maria Eriksdotter, registerhållare för SveDem, professor i geriatrik, Karolinska Institutet, och överläkare på Karolinska Universitetssjukhuset, Huddinge.
Samlar in patientdata
Kvalitetsregistret SveDem – världens största demensregister – samlar en mängd olika data om patienter, från att diagnosen ställs till att personen flyttar till ett särskilt boende. I stort sett alla minnesmottagningar i landet är anslutna men även många vårdcentraler och särskilda boenden registrerar patientdata i SveDem.
De alzheimerläkemedel – kolinesterashämmare och memantin – som idag förskrivs ingick i SveDem redan från registrets startår 2007. De data som analyserats uppvisar små men positiva och långvariga effekter på kognitionen av kolinesterashämmare. Maria Eriksdotter pekar på bland annat en påtagligt lägre mortalitet (dödlighet) jämfört med de som inte har fått kolinesterashämmare förskrivna.
Vad skiljer då den nya läkemedelsmodulen mot det befintliga sättet att registrera läkemedel i SveDem?
Mer detaljerad
– Den nya modulen är betydligt mer detaljerad. Här registreras inte bara när läkemedlet börjar förskrivas, vilken dos och datum för utsättning. Det innehåller även frågor om varför dosen korrigeras, varför läkemedlet sätts ut och så vidare samt uppföljning av kognition och funktion. Till detta kommer de särskilda krav som är förenade med olika läkemedel i framtiden, säger Maria Eriksdotter.
Den svenskutvecklade antikroppen lecanemab kan bli det första nya alzheimerläkemedlet i Sverige på drygt 20 år, om det får klartecken av europeiska läkemedelsmyndigheten (EMA). Efter ett eventuellt godkännande kommer sannolikt att följa en rad villkor för förskrivningen.
– Det kan handla om krav på magnetröntgenundersökning och tätare uppföljningar med instrument som bedömer kognition och funktionsförmåga. Exakt vad det kommer att handla om vet vi ju inte ännu men det är den typen av data som kan registreras och följas upp i den nya modulen, säger Maria Eriksdotter.
Minnesmottagningarna först ut
Lecanemab är inte ett läkemedel som man tar genom munnen. Det ges som dropp varannan vecka och kräver alltså ett besök på en sjukvårdsmottagning.
– Troligen kommer minnesmottagningarna ta hand om detta, om det skulle bli aktuellt. Då är det också minnesmottagningarna som ska registrera i den nya läkemedelsmodulen. Men inget hindrar att vi öppnar modulen även för primärvården, om det skulle behövas, säger Maria Eriksdotter.
Text: Magnus Westlander
Foto (porträtt): David Thunander
Forskningsfynd kan förbättra tidig diagnostik
Forskning från Karolinska Institutet kan öka möjligheterna att ställa tidigare alzheimerdiagnoser. En ny studie visar att proteinet GFPA kan avslöja sjukdomen långt före de första symptomen.
I studien, som publiceras i tidskriften Brain, analyseras blodplasma i släkter med familjär alzheimer. De är bärare av ovanliga ärftliga genmutationer som orsakar Alzheimers sjukdom. Forskarna har samlat in 164 blodplasmaprover mellan 1994 och 2018 från 33 mutationsbärare och 42 släktingar utan det sjukdomsorsakande anlaget.
Resultaten visar tydliga förändringar hos mutationsbärarna när det gäller förekomst av flera olika proteiner i blodet.
10 år före symptom
– Den första förändringen som märktes var en ökning av GFAP (glial fibrillary acidic protein) cirka 10 år före de första sjukdomssymptomen. Den följdes av stegrade värden av P-tau181 och senare NFL (neurofilament light protein), som vi sedan tidigare vet har ett direkt samband med omfattningen av nervcellsskador vid Alzheimers sjukdom, säger Caroline Graff, professor vid institutionen för neurobiologi, vårdvetenskap och samhälle, Karolinska Institutet.
Både P-tau181 och NFL är proteiner som sedan tidigare används som biomarkörer för Alzheimers sjukdom. De kan med relativt god säkerhet upptäcka sjukdomen i ett tidigt skede. Den nya studien tyder på att även GFAP kan fungera som biomarkör vilket kan ytterligare förbättra diagnostiken.
Framsteg inom medicinen
Tidig diagnostik är mer aktuellt än någonsin i och med de senaste framstegen inom medicinen. Den svenskutvecklade antikroppen Lecanemab blev nyligen godkänd som läkemedel i USA. Om Lecanemab även får börja saluföras i Sverige – beslut fattas av den europeiska läkemedelsmyndigheten senare i år – kommer sannolikt patienter i tidig sjukdomsfas att prioriteras vid förskrivningen.
I studien, som publiceras i tidskriften Brain, analyseras blodplasma i släkter med familjär alzheimer. De är bärare av ovanliga ärftliga genmutationer som orsakar Alzheimers sjukdom. Forskarna har samlat in 164 blodplasmaprover mellan 1994 och 2018 från 33 mutationsbärare och 42 släktingar utan det sjukdomsorsakande anlaget.
Resultaten visar tydliga förändringar hos mutationsbärarna när det gäller förekomst av flera olika proteiner i blodet.
10 år före symptom
– Den första förändringen som märktes var en ökning av GFAP (glial fibrillary acidic protein) cirka 10 år före de första sjukdomssymptomen. Den följdes av stegrade värden av P-tau181 och senare NFL (neurofilament light protein), som vi sedan tidigare vet har ett direkt samband med omfattningen av nervcellsskador vid Alzheimers sjukdom, säger Caroline Graff, professor vid institutionen för neurobiologi, vårdvetenskap och samhälle, Karolinska Institutet.
Både P-tau181 och NFL är proteiner som sedan tidigare används som biomarkörer för Alzheimers sjukdom. De kan med relativt god säkerhet upptäcka sjukdomen i ett tidigt skede. Den nya studien tyder på att även GFAP kan fungera som biomarkör vilket kan ytterligare förbättra diagnostiken.
Framsteg inom medicinen
Tidig diagnostik är mer aktuellt än någonsin i och med de senaste framstegen inom medicinen. Den svenskutvecklade antikroppen Lecanemab blev nyligen godkänd som läkemedel i USA. Om Lecanemab även får börja saluföras i Sverige – beslut fattas av den europeiska läkemedelsmyndigheten senare i år – kommer sannolikt patienter i tidig sjukdomsfas att prioriteras vid förskrivningen.
Nyheter från Karolinska Institutet (nytt fönster)
Plasma biomarker profiles in autosomal dominant Alzheimer’s disease, Charlotte Johansson, Steinunn Thordardottir, José Laffita-Mesa, Elena Rodriguez-Vieitez, Henrik Zetterberg, Kaj Blennow och Caroline Graff. Brain, online 11 januari 2023, doi: 10.1093/brain/awac399 (nytt fönster)
Nytt alzheimerläkemedel godkänt i USA
USA:s läkemedelsmyndighet FDA har gett klartecken till försäljning av svenska lecanemab. Alzheimerläkemedlet är det andra som inom två år har godkänts genom ett snabbspår.
Lecanemab har tagits fram av professor Lars Lannfelt i företaget Bioarctic. Utvecklingsarbetet har skett i samarbete med det större läkemedelsbolaget Eisai som nu fått klartecken till att marknadsföra och sälja lecanemab i USA. Det kommer att ske under varumärket Leqembi.
– Det här behandlingsalternativet är den senaste terapin som riktar sig mot och påverkar den underliggande sjukdomsprocessen vid alzheimer, i stället för att bara behandla symtomen på sjukdomen, säger Billy Dunn, avdelningschef vid läkemedelsmyngigehetFDA, i en kommentar till beslutet.
Påverkar placken i hjärnan
Lecanemab är en antikropp som påverkar bland annat de amyloida plack som bildas och sprider sig i en alzheimersjuk hjärna. Det visar en studie på 856 patienter med mild kognitiv funktionsnedsättning eller milda demenssymptom. Gruppen som fick 10 mg/kg lecanemab varannan vecka uppvisade en statistiskt signifikant minskning av amyloida plack under 1,5 år. Motsvarande förändring kunde inte ses i placebogruppen.
Det positiva resultatet får stöd av en nyligen publicerad fas 3-studie som visar att lecanemab ger en 27 procent långsammare försämring av kognitiva funktioner. FDA:s har dock inte hunnit värdera denna studie. Att lecanemab ändå godkänns i USA beror på att det prövats i ett särskilt snabbspår (Accelerated Approval pathway), en möjlighet som finns för läkemedel för allvarliga tillstånd och där det finns ett otillfredsställt medicinskt behov.
Frågetecken finns
Ett frågetecken kring lecanemab är rapporteringen om tre avlidna patienter som använt läkemedlet. Om det finns ett direkt orsakssamband mellan läkemedlet och dödsfallen är fortfarande oklart.
FDA:s förskrivningsinformationen till lecanemab innehåller varningar för biverkningar, bland annat huvudvärk och tillfällig svullnad i delar av hjärnan, som vanligtvis försvinner med tiden.
Enligt Eisai kommer prislappen för lecanemab i USA att ligga på 26 500 US dollar. Vad priset kommmer att bli i Sverige är ännu oklart. Lecanemab måste först godkännas av EMA, den europeiska läkemedelsmyndigheten, innan läkemedelet kan börja marknadsföras och säljas i Sverige.
Lecanemab har tagits fram av professor Lars Lannfelt i företaget Bioarctic. Utvecklingsarbetet har skett i samarbete med det större läkemedelsbolaget Eisai som nu fått klartecken till att marknadsföra och sälja lecanemab i USA. Det kommer att ske under varumärket Leqembi.
– Det här behandlingsalternativet är den senaste terapin som riktar sig mot och påverkar den underliggande sjukdomsprocessen vid alzheimer, i stället för att bara behandla symtomen på sjukdomen, säger Billy Dunn, avdelningschef vid läkemedelsmyngigehetFDA, i en kommentar till beslutet.
Påverkar placken i hjärnan
Lecanemab är en antikropp som påverkar bland annat de amyloida plack som bildas och sprider sig i en alzheimersjuk hjärna. Det visar en studie på 856 patienter med mild kognitiv funktionsnedsättning eller milda demenssymptom. Gruppen som fick 10 mg/kg lecanemab varannan vecka uppvisade en statistiskt signifikant minskning av amyloida plack under 1,5 år. Motsvarande förändring kunde inte ses i placebogruppen.
Det positiva resultatet får stöd av en nyligen publicerad fas 3-studie som visar att lecanemab ger en 27 procent långsammare försämring av kognitiva funktioner. FDA:s har dock inte hunnit värdera denna studie. Att lecanemab ändå godkänns i USA beror på att det prövats i ett särskilt snabbspår (Accelerated Approval pathway), en möjlighet som finns för läkemedel för allvarliga tillstånd och där det finns ett otillfredsställt medicinskt behov.
Frågetecken finns
Ett frågetecken kring lecanemab är rapporteringen om tre avlidna patienter som använt läkemedlet. Om det finns ett direkt orsakssamband mellan läkemedlet och dödsfallen är fortfarande oklart.
FDA:s förskrivningsinformationen till lecanemab innehåller varningar för biverkningar, bland annat huvudvärk och tillfällig svullnad i delar av hjärnan, som vanligtvis försvinner med tiden.
Enligt Eisai kommer prislappen för lecanemab i USA att ligga på 26 500 US dollar. Vad priset kommmer att bli i Sverige är ännu oklart. Lecanemab måste först godkännas av EMA, den europeiska läkemedelsmyndigheten, innan läkemedelet kan börja marknadsföras och säljas i Sverige.
FDA Grants Accelerated Approval for Alzheimer’s Disease Treatment (nytt fönster)
Genombrott för svensk antikropp mot alzheimer (nytt fönster)
Kognitivt test hittar utrikesfödda med demenssymptom
Det kognitiva bedömningsinstrumentet RUDAS-S är bättre än det mer utbredda MMSE på att identifiera utrikesfödda med tidiga demenssymptom. Det visar den första valideringsstudien som gjorts i Sverige.
Rozita Torkpoor, doktorand vid Lunds universitet med en avhandling om Kognitiv utredning av utrikes födda, är en av medförfattarna till studien. Hon är även utvecklare vid Kognition och migration, Region Skåne, och är inte överraskad av resultatet.
RUDAS utvecklades särskilt för att vara opåverkat av testpersonens modersmål, utbildningsnivå och kulturella bakgrund. Det skiljer sig därför från MMSE som är det kognitiva bedömningsinstrument som oftast används vid basala utredningar av misstänkt demenssjukdom.
Orienteringsfrågor problematiska
 Det finns flera delar i MMSE som kan vara problematiska menar Rozita Torkpoor. Det gäller exempelvis orienteringsfrågorna om landskap och årstider.
Det finns flera delar i MMSE som kan vara problematiska menar Rozita Torkpoor. Det gäller exempelvis orienteringsfrågorna om landskap och årstider.
– Du kan ju komma från ett land där det inte finns fyra årstider. Dessutom är frågorna i MMSE svåra att ställa om testledaren och testpersonen inte delar samma språk och även svåra att ställa genom tolk. MMSE förutsätter också att du kan räkna, läsa och skriva vilket gör det olämpligt för personer som har haft en kort skolgång eller inte gått i skolan alls, säger Rozita Torkpoor.
Det här kan leda till fel bedömning av personens kognitiva funktioner. Samma person som testas med RUDAS kan få en högre poäng eftersom detta test är opåverkat av språk eller utbildningsnivå.
Bra på att hitta demens
RUDAS har utvecklats i Australien. Det har översatts och validerats i mer än 20 länder, bland annat Danmark. Valideringen av RUDAS-S, som är namnet på den svenska versionen, har publicerats i Journal of Alzheimer’s Disease . I studien ingick 123 patienter, både utrikesfödda och svenskfödda. Resultatet visade att testet hade en god förmåga att upptäcka demens hos samtliga patienter oavsett ursprungsland.
– Testet hade en hög sensitivitet, 0,92 (1,0 är högst red. anm.). Det är ett högt värde och betyder att RUDAS-S är bra på att hitta personer med demenssjukdom, säger Rozita Torkpoor.
RUDAS är, precis som MMSE, ett globalt screeningsinstrument som ger en samlad bedömning av hjärnans funktion. I praktiken behöver man oftast även kompletterande tester som mer specifikt kan utvärdera olika kognitiva funktioner.
Mångkulturellt test
För närvarande arbetar Rozita Torkpoor med att validera MCE-S, som är den svenska versionen av testet Multicutural Cognitive Examination. Det är ett mångkulturellt kognitivt test som omfattar RUDAS och tre andra test som bedömer minne, språkförmåga och visuospatial förmåga.
Med delfinansiering från innovationsmiljön PREDEM har enheten Kognition och migration i Region Skåne anställt en sjuksköterska som har startat ett utvecklingsarbete inom primärvården med hjälp av tio skånska vårdcentraler.
– Vi både utbildar och stöttar arbetsterapeuter, sjuksköterskor och läkare i användningen av MCE-S. Projektet följs upp för att bland annat se om MCE-S kan underlätta och förbättra diagnostiken inom primärvården. Resultatet publiceras under nästa år, säger Rozita Torkpoor.
Magnus Westlander
Diagnostic Accuracy of the Swedish Version of the Rowland Universal Dementia Assessment Scale (RUDAS-S) for Multicultural Cognitive Screening in Swedish Memory Clinics. Rozita Torkpoor, Kristin Frolich, T. Rune Nielsen and Elisabet Londos, Lunds universitet. Journal of Alzheimer’s Disease 89 (2022) 865–876. jad220233 – iospress.com (nytt fönster)
Rozita Torkpoor, doktorand vid Lunds universitet med en avhandling om Kognitiv utredning av utrikes födda, är en av medförfattarna till studien. Hon är även utvecklare vid Kognition och migration, Region Skåne, och är inte överraskad av resultatet.
RUDAS utvecklades särskilt för att vara opåverkat av testpersonens modersmål, utbildningsnivå och kulturella bakgrund. Det skiljer sig därför från MMSE som är det kognitiva bedömningsinstrument som oftast används vid basala utredningar av misstänkt demenssjukdom.
Orienteringsfrågor problematiska
 Det finns flera delar i MMSE som kan vara problematiska menar Rozita Torkpoor. Det gäller exempelvis orienteringsfrågorna om landskap och årstider.
Det finns flera delar i MMSE som kan vara problematiska menar Rozita Torkpoor. Det gäller exempelvis orienteringsfrågorna om landskap och årstider.
– Du kan ju komma från ett land där det inte finns fyra årstider. Dessutom är frågorna i MMSE svåra att ställa om testledaren och testpersonen inte delar samma språk och även svåra att ställa genom tolk. MMSE förutsätter också att du kan räkna, läsa och skriva vilket gör det olämpligt för personer som har haft en kort skolgång eller inte gått i skolan alls, säger Rozita Torkpoor.
Det här kan leda till fel bedömning av personens kognitiva funktioner. Samma person som testas med RUDAS kan få en högre poäng eftersom detta test är opåverkat av språk eller utbildningsnivå.
Bra på att hitta demens
RUDAS har utvecklats i Australien. Det har översatts och validerats i mer än 20 länder, bland annat Danmark. Valideringen av RUDAS-S, som är namnet på den svenska versionen, har publicerats i Journal of Alzheimer’s Disease . I studien ingick 123 patienter, både utrikesfödda och svenskfödda. Resultatet visade att testet hade en god förmåga att upptäcka demens hos samtliga patienter oavsett ursprungsland.
– Testet hade en hög sensitivitet, 0,92 (1,0 är högst red. anm.). Det är ett högt värde och betyder att RUDAS-S är bra på att hitta personer med demenssjukdom, säger Rozita Torkpoor.
RUDAS är, precis som MMSE, ett globalt screeningsinstrument som ger en samlad bedömning av hjärnans funktion. I praktiken behöver man oftast även kompletterande tester som mer specifikt kan utvärdera olika kognitiva funktioner.
Mångkulturellt test
För närvarande arbetar Rozita Torkpoor med att validera MCE-S, som är den svenska versionen av testet Multicutural Cognitive Examination. Det är ett mångkulturellt kognitivt test som omfattar RUDAS och tre andra test som bedömer minne, språkförmåga och visuospatial förmåga.
Med delfinansiering från innovationsmiljön PREDEM har enheten Kognition och migration i Region Skåne anställt en sjuksköterska som har startat ett utvecklingsarbete inom primärvården med hjälp av tio skånska vårdcentraler.
– Vi både utbildar och stöttar arbetsterapeuter, sjuksköterskor och läkare i användningen av MCE-S. Projektet följs upp för att bland annat se om MCE-S kan underlätta och förbättra diagnostiken inom primärvården. Resultatet publiceras under nästa år, säger Rozita Torkpoor.
Magnus Westlander
Diagnostic Accuracy of the Swedish Version of the Rowland Universal Dementia Assessment Scale (RUDAS-S) for Multicultural Cognitive Screening in Swedish Memory Clinics. Rozita Torkpoor, Kristin Frolich, T. Rune Nielsen and Elisabet Londos, Lunds universitet. Journal of Alzheimer’s Disease 89 (2022) 865–876. jad220233 – iospress.com (nytt fönster)
• RUDAS står för Rowland Universal Dementia Assessment Scale och är ett kognitivt bedömningsinstrument (screeningsinstrument).
• RUDAS rekommenderas i Socialstyrelsen nationella riktlinjer som en del i en basal demensutredning av personer med misstänkt demenssjukdom och annat modersmål än svenska eller annan kulturell bakgrund.
• RUDAS-S, den svenska versionen, kan laddas ned avgiftsfritt från Region Skånes webbplats (nytt fönster).
Genombrott för svensk antikropp mot alzheimer
Blir en antikropp utvecklad vid Uppsala universitet det första nya alzheimerläkemedlet i Europa på över 20 år? Hoppfulla resultat från en läkemedelsprövning tyder på det.
Det är läkemedelsbolaget Eisai som i ett pressmeddelande redovisar en fas 3-studie på Lecanemab. Den omfattar 1795 deltagare med alzheimer i tidig sjukdomsfas. Cirka hälften av dem fick Lecanemab under 18 månader, övriga deltare ingick i en kontrollgrupp.
Resultaten, som enligt Eisai är statistiskt säkerställda, visar att Lecanemab gav en långsammare försämring av kognitiva funktioner motsvarande 27 procent. Läkemedlets positiva effekter uppmättes redan efter ett halvår och kvarstod under 18 månader då studien avslutades. Biverkningar, i form av hjärnsvullnad, förekom hos 12,5 procent. Men endast 2,8 procent hade symptom av detta.
Ett glädjebud
– Beskedet är ett glädjebud. Resultaten verkar vara tydliga och odiskutabla. Detta är otroligt viktigt för alzheimerforskningen, säger Bengt Winblad, professor vid Karolinska institutet, i Dagens medicin.
Forskarvärlden har ännu inte hunnit granska studien som väntar på att publiceras i en vetenskaplig tidskrift. Men både Bengt Winblad och Kaj Blennow, professor vid Göteborgs universitet, räknar med att resultaten gör att EU:s läkemedelsmyndighet EMA kommer att godkänna Lecanemab.
– Jag bedömer bromseffekten i studien på 27 procent som kliniskt relevant. När patienterna i klinisk praxis behandlas under längre tid än som var fallet i studien kommer effekten troligen bli tydligare, säger Kaj Blennow till Dagens medicin.
Utvecklad vid Uppsala universitet
 Lecanemab bygger på BAN2401, en antikropp som Lars Lannfelt, professor vid Uppsala universitet, utvecklat i sitt bolag BioArctic som är samarbetspartner till Eisai. BAN2401 måltavla är de giftiga oligomererna. De utgör ett slags mellanstadium i utveckling av de amyloida plack som lagras i hjärnan vid Alzheimers sjukdom.
Lecanemab bygger på BAN2401, en antikropp som Lars Lannfelt, professor vid Uppsala universitet, utvecklat i sitt bolag BioArctic som är samarbetspartner till Eisai. BAN2401 måltavla är de giftiga oligomererna. De utgör ett slags mellanstadium i utveckling av de amyloida plack som lagras i hjärnan vid Alzheimers sjukdom.
Tidigare försök med antikroppar mot alzheimer har misslyckats med undantag av Aduhelm. Den har godkänts som läkemedel i USA men inte i Europa. EMA, europeiska läkemedelsmyndigheten, ansåg att det fanns stora frågetecken kring de positiva effekterna för patienterna.
Eisai hoppas kunna få Lecanemab prövat som läkemedel i USA, Japan och Europa i slutet av mars 2023.
Det är läkemedelsbolaget Eisai som i ett pressmeddelande redovisar en fas 3-studie på Lecanemab. Den omfattar 1795 deltagare med alzheimer i tidig sjukdomsfas. Cirka hälften av dem fick Lecanemab under 18 månader, övriga deltare ingick i en kontrollgrupp.
Resultaten, som enligt Eisai är statistiskt säkerställda, visar att Lecanemab gav en långsammare försämring av kognitiva funktioner motsvarande 27 procent. Läkemedlets positiva effekter uppmättes redan efter ett halvår och kvarstod under 18 månader då studien avslutades. Biverkningar, i form av hjärnsvullnad, förekom hos 12,5 procent. Men endast 2,8 procent hade symptom av detta.
Ett glädjebud
– Beskedet är ett glädjebud. Resultaten verkar vara tydliga och odiskutabla. Detta är otroligt viktigt för alzheimerforskningen, säger Bengt Winblad, professor vid Karolinska institutet, i Dagens medicin.
Forskarvärlden har ännu inte hunnit granska studien som väntar på att publiceras i en vetenskaplig tidskrift. Men både Bengt Winblad och Kaj Blennow, professor vid Göteborgs universitet, räknar med att resultaten gör att EU:s läkemedelsmyndighet EMA kommer att godkänna Lecanemab.
– Jag bedömer bromseffekten i studien på 27 procent som kliniskt relevant. När patienterna i klinisk praxis behandlas under längre tid än som var fallet i studien kommer effekten troligen bli tydligare, säger Kaj Blennow till Dagens medicin.
Utvecklad vid Uppsala universitet
 Lecanemab bygger på BAN2401, en antikropp som Lars Lannfelt, professor vid Uppsala universitet, utvecklat i sitt bolag BioArctic som är samarbetspartner till Eisai. BAN2401 måltavla är de giftiga oligomererna. De utgör ett slags mellanstadium i utveckling av de amyloida plack som lagras i hjärnan vid Alzheimers sjukdom.
Lecanemab bygger på BAN2401, en antikropp som Lars Lannfelt, professor vid Uppsala universitet, utvecklat i sitt bolag BioArctic som är samarbetspartner till Eisai. BAN2401 måltavla är de giftiga oligomererna. De utgör ett slags mellanstadium i utveckling av de amyloida plack som lagras i hjärnan vid Alzheimers sjukdom.
Tidigare försök med antikroppar mot alzheimer har misslyckats med undantag av Aduhelm. Den har godkänts som läkemedel i USA men inte i Europa. EMA, europeiska läkemedelsmyndigheten, ansåg att det fanns stora frågetecken kring de positiva effekterna för patienterna.
Eisai hoppas kunna få Lecanemab prövat som läkemedel i USA, Japan och Europa i slutet av mars 2023.
Pressmeddelande från Eisai (nytt fönster)
Artikel i Dagens medicin (nytt fönster)
Lovande resultat med ny biomarkör
Forskningen om biomarkörer går stadigt framåt. Inom ramen för innovationsmiljön PREDEM studerar forskarna glykaner, ett ganska outforskat ämne som de hoppas kan bidra till att upptäcka Alzheimers sjukdom redan innan symptomen uppträder.
– Det ser riktigt lovande ut. Jag tror att vår glykanstruktur kan bli ett bra komplement till andra biomakörer, säger Sophia Schedin Weiss, docent i biokemi, som tillsammans med sina forskarkollegor vid Karolinska Institutet just har sammanställt resultatet av en mindre studie med 255 personer.
Glykaner är olika sockermolekyler som finns på ytan av kroppens byggstenar: proteinerna. Glykaner finns på de flesta proteiner och fungerar bland annat som adresslappar. De visar var i kroppen proteinet ska finnas och hur det ska fungera.
Betydelsen underskattad
 – Ett och samma protein som bildas i olika delar av kroppen har olika glykanstrukturer vilket gör att de får helt olika funktion, säger Sophia Schedin Weiss som anser att glykaners betydelse är större än vad många forskare är medvetna om.
– Ett och samma protein som bildas i olika delar av kroppen har olika glykanstrukturer vilket gör att de får helt olika funktion, säger Sophia Schedin Weiss som anser att glykaners betydelse är större än vad många forskare är medvetna om.
– Men ska man ta hänsyn till glykaner blir proteinanalyserna mer komplicerade. Då är det lättare att blunda för dem. Forskningsanslagen förutsätter ofta snabba resultat, säger hon.
Sophia Schedin Weiss fick upp ögonen för glykaner redan som doktorand, ett intresse som har hållit i sig. Numera analyserar hon glykaner av en viss typ i alla de proteiner som finns i ryggvätska. En av glykanstrukturerna har visat sig vara betydligt vanligare vid Alzheimers sjukdom.
Koppling till annan biomarkör
– Vi har jämfört vår glykanstruktur med andra biomarkörer och hittat en korrelation med proteinet tau (total-tau red.anm.), det är särskilt tydligt i gruppen med lindrig kognitiv nedsättning (MCI) som ju ofta är ett förstadium till alzheimer, säger Sophia Schedin Weiss.
Tau är det protein som vid alzheimer veckar sig inne i hjärncellerna och som leder till att hjärnvävnad dör. Olika former av tau används därför som biomarkörer. Genom att mäta förekomsten av tau i ryggvätska kan man med relativt god säkerhet förutsäga om personen kommer att utveckla alzheimer. Numera kan man även med i stort sett samma tillförlitlighet få ut samma information om alzheimerutvecklingen ur en droppe blod.
– Vår nyligen avslutade glykanstudie bygger på just blodanalyser från 255 personer i SNACK. Det är en longitidunell kohortstudie där personerna har undersökts och lämnat prover regelbundet under många år. Den starka korrelation mellan total-tau och vår glykanstruktur som vi tidigare såg i ryggvätska fanns även här, säger Sophia Schedin Weiss.
Blodanalysen tillförlitlig
Hon tycker resultatet lovar gott. Glykanstrukturen tycks fånga upp alzheimerförändringar som sker väldigt tidigt i sjukdomsutvecklingen. Dessutom verkar blodanalysen lika tillförlitlig som analysen från ryggvätska. Den senare är dyrare och tillgängligt endast på vissa specialistkliniker.
– Nästa steg blir att testa glykanstrukturen i större skala. Det kommmer att ske i en primärvårdsstudie som också görs inom ramen för PREDEM. I den kommer man också mäta andra biomarkörer, säger Sophia Schedin Weiss.
Men varför behöver vi fler biomarkörer?
Urskilja olika alzheimertyper
– Forskningen kommer knappast att hitta endast en biomarkör som säkert kan påvisa en framtida alzheimerutveckling. Dessutom, ju fler biomarkörer vi har desto större möjlighet att urskilja olika subtyper av alzheimer. Det handlar om precisionsdiagnostik som ju också är ett viktigt mål för PREDEM, säger Sophia Schedin Weiss.
Text: Magnus Westlander
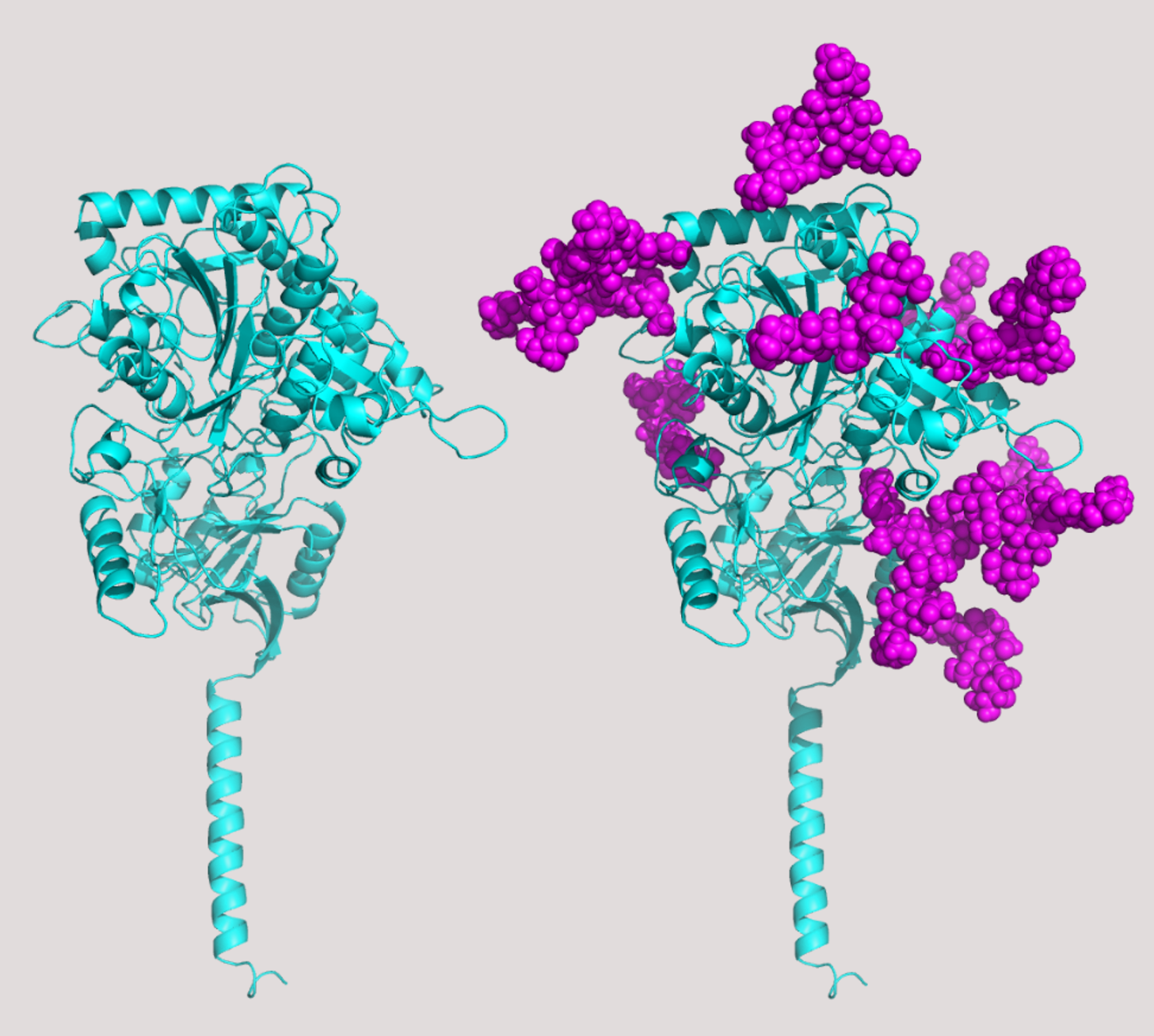
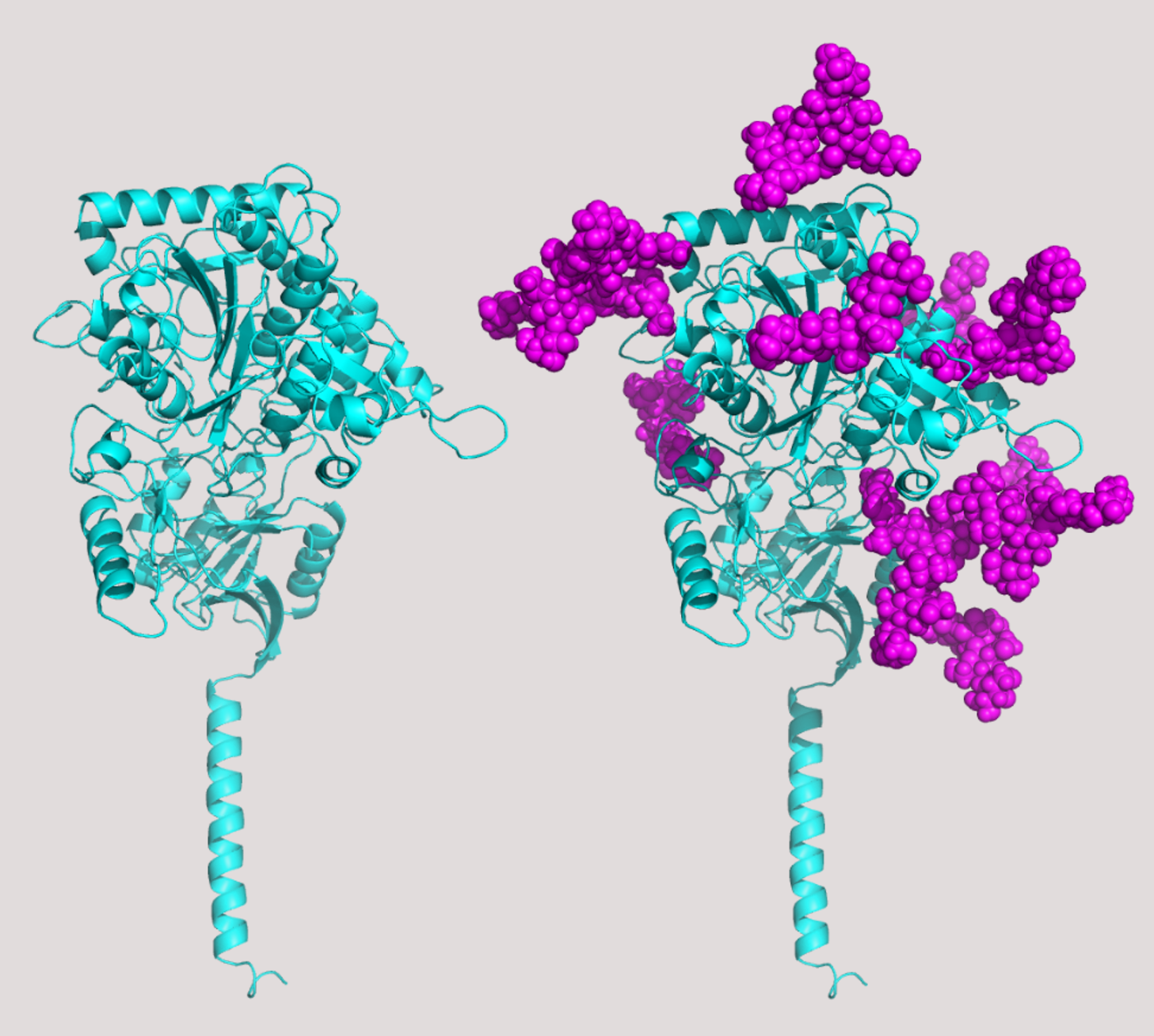 Bild på glykan. Visar glukanstrukturen för nicastrin som är en del av gammasekretas – ett enzym som behövs för att Abeta ska bildas. I högra bilden har 11 av 16 potentiella N-glykaner (magentafärg) på nicastrin (cyan) modellerats för att visa hur stor del glykaner kan uppta av ett proteins yta.
Bild på glykan. Visar glukanstrukturen för nicastrin som är en del av gammasekretas – ett enzym som behövs för att Abeta ska bildas. I högra bilden har 11 av 16 potentiella N-glykaner (magentafärg) på nicastrin (cyan) modellerats för att visa hur stor del glykaner kan uppta av ett proteins yta.
– Det ser riktigt lovande ut. Jag tror att vår glykanstruktur kan bli ett bra komplement till andra biomakörer, säger Sophia Schedin Weiss, docent i biokemi, som tillsammans med sina forskarkollegor vid Karolinska Institutet just har sammanställt resultatet av en mindre studie med 255 personer.
Glykaner är olika sockermolekyler som finns på ytan av kroppens byggstenar: proteinerna. Glykaner finns på de flesta proteiner och fungerar bland annat som adresslappar. De visar var i kroppen proteinet ska finnas och hur det ska fungera.
Betydelsen underskattad
 – Ett och samma protein som bildas i olika delar av kroppen har olika glykanstrukturer vilket gör att de får helt olika funktion, säger Sophia Schedin Weiss som anser att glykaners betydelse är större än vad många forskare är medvetna om.
– Ett och samma protein som bildas i olika delar av kroppen har olika glykanstrukturer vilket gör att de får helt olika funktion, säger Sophia Schedin Weiss som anser att glykaners betydelse är större än vad många forskare är medvetna om.
– Men ska man ta hänsyn till glykaner blir proteinanalyserna mer komplicerade. Då är det lättare att blunda för dem. Forskningsanslagen förutsätter ofta snabba resultat, säger hon.
Sophia Schedin Weiss fick upp ögonen för glykaner redan som doktorand, ett intresse som har hållit i sig. Numera analyserar hon glykaner av en viss typ i alla de proteiner som finns i ryggvätska. En av glykanstrukturerna har visat sig vara betydligt vanligare vid Alzheimers sjukdom.
Koppling till annan biomarkör
– Vi har jämfört vår glykanstruktur med andra biomarkörer och hittat en korrelation med proteinet tau (total-tau red.anm.), det är särskilt tydligt i gruppen med lindrig kognitiv nedsättning (MCI) som ju ofta är ett förstadium till alzheimer, säger Sophia Schedin Weiss.
Tau är det protein som vid alzheimer veckar sig inne i hjärncellerna och som leder till att hjärnvävnad dör. Olika former av tau används därför som biomarkörer. Genom att mäta förekomsten av tau i ryggvätska kan man med relativt god säkerhet förutsäga om personen kommer att utveckla alzheimer. Numera kan man även med i stort sett samma tillförlitlighet få ut samma information om alzheimerutvecklingen ur en droppe blod.
– Vår nyligen avslutade glykanstudie bygger på just blodanalyser från 255 personer i SNACK. Det är en longitidunell kohortstudie där personerna har undersökts och lämnat prover regelbundet under många år. Den starka korrelation mellan total-tau och vår glykanstruktur som vi tidigare såg i ryggvätska fanns även här, säger Sophia Schedin Weiss.
Blodanalysen tillförlitlig
Hon tycker resultatet lovar gott. Glykanstrukturen tycks fånga upp alzheimerförändringar som sker väldigt tidigt i sjukdomsutvecklingen. Dessutom verkar blodanalysen lika tillförlitlig som analysen från ryggvätska. Den senare är dyrare och tillgängligt endast på vissa specialistkliniker.
– Nästa steg blir att testa glykanstrukturen i större skala. Det kommmer att ske i en primärvårdsstudie som också görs inom ramen för PREDEM. I den kommer man också mäta andra biomarkörer, säger Sophia Schedin Weiss.
Men varför behöver vi fler biomarkörer?
Urskilja olika alzheimertyper
– Forskningen kommer knappast att hitta endast en biomarkör som säkert kan påvisa en framtida alzheimerutveckling. Dessutom, ju fler biomarkörer vi har desto större möjlighet att urskilja olika subtyper av alzheimer. Det handlar om precisionsdiagnostik som ju också är ett viktigt mål för PREDEM, säger Sophia Schedin Weiss.
Text: Magnus Westlander
 Bild på glykan. Visar glukanstrukturen för nicastrin som är en del av gammasekretas – ett enzym som behövs för att Abeta ska bildas. I högra bilden har 11 av 16 potentiella N-glykaner (magentafärg) på nicastrin (cyan) modellerats för att visa hur stor del glykaner kan uppta av ett proteins yta.
Bild på glykan. Visar glukanstrukturen för nicastrin som är en del av gammasekretas – ett enzym som behövs för att Abeta ska bildas. I högra bilden har 11 av 16 potentiella N-glykaner (magentafärg) på nicastrin (cyan) modellerats för att visa hur stor del glykaner kan uppta av ett proteins yta.
Uppsalaprofessor prisas för sin alzheimerforskning
Svenska Läkaresällskapet har tilldelat professor Lars Lannfelt Bengt Winblads pris 2022. Han får de för framstående insatser inom molekylär geriatrik som lett till en ökad förståelse för hur Alzheimers sjukdom utvecklas.
Professor Lars Lannfelt ingår i forskningsgruppen för Molekylär Geriatrik, en del av Geriatrik vid Uppsala universitet. Gruppen arbetar för att utveckla metoder för både tidig diagnostik och förebyggande behandling av alzheimer.
Banbrytande upptäckt
Under slutet av 1990-talet gjorde Lars Lannfelt en banbrytande upptäck då han fann den Arktiska mutationen hos en släkt i övre Norrland. Mutationen leder till ökade nivåer av giftiga Aβ-protofibriller som orsakar nervcellsdöd och slutligen Alzheimers sjukdom.
Baserat på dessa resultat grundade Lars Lannfelt bolaget BioArctic som utvecklat antikroppen BAN2401, en internationellt mycket uppmärksammad läkemedelskandidat mot alzheimer.
Framgångsrika studier
– Det är med stor glädje som vår forskning uppmärksammas och belönas med Bengt Winblads pris. Genom att använda Aβ-protofibriller som måltavla har vi lyckats ta fram en antikroppsbaserad behandling mot Alzheimers sjukdom. De inledande studierna har varit framgångsrika och en antikropp prövas nu i kliniska studier, fas III, säger Lars Lannfelt i ett pressmeddelande från Svenska Läkaresällskapet (nytt fönster).
Professor Lars Lannfelt ingår i forskningsgruppen för Molekylär Geriatrik, en del av Geriatrik vid Uppsala universitet. Gruppen arbetar för att utveckla metoder för både tidig diagnostik och förebyggande behandling av alzheimer.
Banbrytande upptäckt
Under slutet av 1990-talet gjorde Lars Lannfelt en banbrytande upptäck då han fann den Arktiska mutationen hos en släkt i övre Norrland. Mutationen leder till ökade nivåer av giftiga Aβ-protofibriller som orsakar nervcellsdöd och slutligen Alzheimers sjukdom.
Baserat på dessa resultat grundade Lars Lannfelt bolaget BioArctic som utvecklat antikroppen BAN2401, en internationellt mycket uppmärksammad läkemedelskandidat mot alzheimer.
Framgångsrika studier
– Det är med stor glädje som vår forskning uppmärksammas och belönas med Bengt Winblads pris. Genom att använda Aβ-protofibriller som måltavla har vi lyckats ta fram en antikroppsbaserad behandling mot Alzheimers sjukdom. De inledande studierna har varit framgångsrika och en antikropp prövas nu i kliniska studier, fas III, säger Lars Lannfelt i ett pressmeddelande från Svenska Läkaresällskapet (nytt fönster).
Bakslag för antikropp mot alzheimer
I drygt tio år har en antikropp mot alzheimer testats på personer i en colombiansk släkt. Men förhoppningarna, att kunna förebygga den ärftliga formen av sjukdomen som finns i släkten, har tyvärr inte infriats.
Resultatet av denna preventionsstudie presenterades nyligen av läkemedelsbolaget Roche vid den stora AAIC-konferensen i Basel. I ett pressmeddelande slår bolaget fast att antikroppen crenezumab varken kunde förhindra eller dämpa kognitiv försämring. I studien ingick 252 deltagare.
Roche har samarbetat med bland andra Banner Alzheimer’s Institute och University of Antioquia in Colombia. Studien har rönt stort intresse eftersom antikroppen crenezumab prövats på deltagare som, när försöket inleddes, inte hade utvecklat några alzheimersymptom. Deltagarna kommer från en stor colombiansk släkt där en ärftlig mutation är utbredd och är en direkt orsak till Alzheimers sjukdom. De som bär på detta anlag insjuknar redan i 40-årsåldern.
Många bedömare anser att tidigare läkemedelsprövningar kan ha misslyckats eftersom antikropparna satts in för sent, när personerna redan utvecklat tydliga alzheimersymptom. Men inte heller i den colombianska studien kunde alzheimer förebyggas eller fördröjas. Antikroppen crenezumab har tidigare testats vid sporadisk (icke-ärftlig) alzheimer med samma negativa resultat.
Resultatet av denna preventionsstudie presenterades nyligen av läkemedelsbolaget Roche vid den stora AAIC-konferensen i Basel. I ett pressmeddelande slår bolaget fast att antikroppen crenezumab varken kunde förhindra eller dämpa kognitiv försämring. I studien ingick 252 deltagare.
Roche har samarbetat med bland andra Banner Alzheimer’s Institute och University of Antioquia in Colombia. Studien har rönt stort intresse eftersom antikroppen crenezumab prövats på deltagare som, när försöket inleddes, inte hade utvecklat några alzheimersymptom. Deltagarna kommer från en stor colombiansk släkt där en ärftlig mutation är utbredd och är en direkt orsak till Alzheimers sjukdom. De som bär på detta anlag insjuknar redan i 40-årsåldern.
Många bedömare anser att tidigare läkemedelsprövningar kan ha misslyckats eftersom antikropparna satts in för sent, när personerna redan utvecklat tydliga alzheimersymptom. Men inte heller i den colombianska studien kunde alzheimer förebyggas eller fördröjas. Antikroppen crenezumab har tidigare testats vid sporadisk (icke-ärftlig) alzheimer med samma negativa resultat.
Pressmeddelande från Roche (nytt fönster)
Blodprov kan upptäcka alzheimer vid Downs syndrom
En studie från Lunds universitet visar att alzheimer hos personer med Downs syndrom med stor säkerhet kan upptäckas genom ett enkelt blodprov. Det nya fyndet gör det möjligt att ställa korrekta diagnoser utan större ingrepp.
Alzheimers sjukdom är den vanligaste dödsorsaken hos personer med Downs syndrom. Ca 80 procent av dem utvecklar sjukdomen, ofta redan i 40-, 50-årsåldern. Alzheimer kan dock vara svår att upptäcka och diagnosticera, bland annat eftersom personerna bär med sig kognitiva funktionsnedsättningar redan från födseln.
Stor säkerhet
Nu visar en svensk-amerikansk studie, ledd från Lunds universitet, att ett enkelt blodprov med stor säkerhet kan upptäcka Alzheimers sjukdom hos personer med Downs syndrom. Forskarna har jämfört en biomarkör genom blodprov med resultat från en mer omfattande PET-kameraundersökning. Studien omfattade 300 personer med Downs syndrom av vilka 40 procent visade tecken på begynnande Alzheimers sjukdom.
– Med det enkla blodprovet kunde vi med över 90 procents säkerhet upptäcka både tau- och amyloidpatologier, det vill säga de sjukdomsframkallande förändringar i hjärnan som visar om en person har alzheimer eller ej. Vi kunde även ställa diagnos på dem som ännu inte utvecklat tydlig kognitiv svikt på grund av Alzheimers sjukdom, säger Oskar Hansson, professor i neurologi vid Lunds universitet och överläkare vid minnesmottagningen på Skånes universitetssjukhus, i ett pressmeddelande.
Undvika stora ingrepp
Fynden är viktiga av flera skäl. Med ett enkelt blodprov ökar möjligheterna att ställa korrekt diagnos utan att behöva göra mer invasiva och kostsamma ingrepp som till exempel ett ryggvätskeprov innebär
För ett par år sedan presenterade Oskar Hansson och hans forskarkollegor ett genombrott inom alzheimerdiagnostiken: att en biomarkör i blodet kan påvisa Alzheimers sjukdom redan 20 år innan minnesbesvär blir tydliga och urskilja Alzheimers sjukdom från andra demenssjukdomar med cirka 95 procents noggrannhet. Samma biomarkör, fosforylerat tau217, har använts i den aktuella studien.
– Nästa steg är att utvärdera detta i klinisk praxis och även använda det för att förbättra läkemedelsprövningar som utvärderar läkemedel riktade mot alzheimer hos personer med Downs syndrom, säger Oskar Hansson.
Alzheimers sjukdom är den vanligaste dödsorsaken hos personer med Downs syndrom. Ca 80 procent av dem utvecklar sjukdomen, ofta redan i 40-, 50-årsåldern. Alzheimer kan dock vara svår att upptäcka och diagnosticera, bland annat eftersom personerna bär med sig kognitiva funktionsnedsättningar redan från födseln.
Stor säkerhet
Nu visar en svensk-amerikansk studie, ledd från Lunds universitet, att ett enkelt blodprov med stor säkerhet kan upptäcka Alzheimers sjukdom hos personer med Downs syndrom. Forskarna har jämfört en biomarkör genom blodprov med resultat från en mer omfattande PET-kameraundersökning. Studien omfattade 300 personer med Downs syndrom av vilka 40 procent visade tecken på begynnande Alzheimers sjukdom.
– Med det enkla blodprovet kunde vi med över 90 procents säkerhet upptäcka både tau- och amyloidpatologier, det vill säga de sjukdomsframkallande förändringar i hjärnan som visar om en person har alzheimer eller ej. Vi kunde även ställa diagnos på dem som ännu inte utvecklat tydlig kognitiv svikt på grund av Alzheimers sjukdom, säger Oskar Hansson, professor i neurologi vid Lunds universitet och överläkare vid minnesmottagningen på Skånes universitetssjukhus, i ett pressmeddelande.
Undvika stora ingrepp
Fynden är viktiga av flera skäl. Med ett enkelt blodprov ökar möjligheterna att ställa korrekt diagnos utan att behöva göra mer invasiva och kostsamma ingrepp som till exempel ett ryggvätskeprov innebär
För ett par år sedan presenterade Oskar Hansson och hans forskarkollegor ett genombrott inom alzheimerdiagnostiken: att en biomarkör i blodet kan påvisa Alzheimers sjukdom redan 20 år innan minnesbesvär blir tydliga och urskilja Alzheimers sjukdom från andra demenssjukdomar med cirka 95 procents noggrannhet. Samma biomarkör, fosforylerat tau217, har använts i den aktuella studien.
– Nästa steg är att utvärdera detta i klinisk praxis och även använda det för att förbättra läkemedelsprövningar som utvärderar läkemedel riktade mot alzheimer hos personer med Downs syndrom, säger Oskar Hansson.
Orsaken till att personer med Downs Syndrom utvecklar Alzheimers sjukdom i relativt hög utsträckning är att de har en extra kromosom, tre exemplar av kromosom 21 istället för två. Den gen som kodar för APP (amyloid prekursorproteinet), det vill säga det protein som bildar amyloid, finns på just kromosom 21. Vid Downs syndrom bildar man mer av APP och har därmed en klart ökad risk att få amyloida aggregat (klumpar) som i sin tur leder till aggregat av tau.
Källa: Lunds universitet
Innovationsmiljö ska förebygga demenssjukdom
Innovationsmiljön PREDEM är inne på sitt första halvår. Vi bad initiativtagaren Linus Jönsson, docent i hälsoekonomi vid Karolinska Institutet, berätta hur det går och hur PREDEM ska kunna bidra till att förebygga demenssjukdom.
 Som en av elva innovationsmiljöer får PREDEM finansiering av statliga Vinnova under fem år. I PREDEM:s fall är siktet intsälllt på att utveckla diagnostik, precisionsmedicin och beslutsstöd, allt för att förebygga demensutveckling hos personer med begynnande kognitiv svikt.
Som en av elva innovationsmiljöer får PREDEM finansiering av statliga Vinnova under fem år. I PREDEM:s fall är siktet intsälllt på att utveckla diagnostik, precisionsmedicin och beslutsstöd, allt för att förebygga demensutveckling hos personer med begynnande kognitiv svikt.
PREDEM samlar flera olika aktörer från akademi, region och företag. Här deltar även Svenskt Demenscentrum som på sin webbplats kommer att spegla arbetet inom PREDEM och de framsteg som görs.
Spännande studier ligger i pipeline, intervju med Linus Jönsson!
 Som en av elva innovationsmiljöer får PREDEM finansiering av statliga Vinnova under fem år. I PREDEM:s fall är siktet intsälllt på att utveckla diagnostik, precisionsmedicin och beslutsstöd, allt för att förebygga demensutveckling hos personer med begynnande kognitiv svikt.
Som en av elva innovationsmiljöer får PREDEM finansiering av statliga Vinnova under fem år. I PREDEM:s fall är siktet intsälllt på att utveckla diagnostik, precisionsmedicin och beslutsstöd, allt för att förebygga demensutveckling hos personer med begynnande kognitiv svikt.
PREDEM samlar flera olika aktörer från akademi, region och företag. Här deltar även Svenskt Demenscentrum som på sin webbplats kommer att spegla arbetet inom PREDEM och de framsteg som görs.
Spännande studier ligger i pipeline, intervju med Linus Jönsson!